Серная кислота
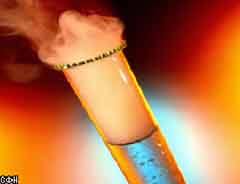
Серная кислота H2SO4 - одна из сильных двухосновных кислот. В разбавленном состоянии она окисляет почти все металлы, кроме золота и платины. Интенсивно реагирует с неметаллами и органическими веществами, превращая некоторые из них в уголь. При приготовлении раствора серной кислоты всегда надо её приливать к воде, а не наоборот, во избежание разбрызгивания и вскипания воды. При 10 °С затвердевает, образуя прозрачную стекловидную массу. При нагревании 100-процентная серная кислота легко теряет серный ангидрид (триокись серы SO3) до тех пор, пока её концентрация не составит 98 %. Именно в таком состоянии её обычно и используют в лабораториях. В концентрированном (безводном) состоянии серная кислота - бесцветная, дымящаяся на воздухе (из-за паров), маслянистая жидкость с характерным запахом (Т кипения=338 °С). Она является очень сильным окислителем. Это вещество обладает всеми свойствами кислот:
Химические свойства серной кислоты
- химическая реакция с металлами:
H2SO4 + Fe → FeSO4 + H2;
2H2SO4 + Cu → CuSO4 + SO2 +2H2O - в этом случае кислота является концентрированной.
- химическая реакция с оксидами металлов:
H2SO4 + CuO → CuSO4 + H2O
Получающийся раствор синего цвета - CuSO4 - раствор медного купороса. Серную кислоту еще называют купоросным маслом, так как при реакциях с металлами и их оксидами образуются купоросы. Например, при химической реакции с железом (Fe) - образуется светло-зелёный раствор железного купороса.
- химическая реакция с основаниями и щелочами (или реакция нейтрализации)
H2SO4 + 2NaOH → Na2SO4 + 2H2O
- химическая реакция с серой (кислота - концентрированная, реакция - при нагревании):
2H2SO4 + S → 3SO2 + 2H2O
- химическая реакция с солями (например, со стиральной содой Na2CO3):
H2SO4 + Na2CO3 → Na2SO4 + CO2 + H2O
Получение серной кислоты

Серную кислоту получают окислением серы (S) сначала до оксида серы (сернистого газа SO2), а затем окислением сернистого газа до триоксида серы (сернистого ангидрида SO3) (на рисунке слева):
S + O2 → SO2
- сернистый газ - с удушливым запахом
серы.
SO2 + O2 → SO3. Эта химическая реакция производится на катализаторе (оксиде ванадия V2O5). Вещество SO3 - сернистый ангидрид - очень гигроскопичное кристаллическое прозрачное вещество, жадно поглощающее воду с образованием серной кислоты:
SO3 + H2O → H2SO4
Сернистая кислота
Сернистая кислота - или Н2SO3 - так называют водный раствор оксида серы (SO2) в воде. На самом деле такого химического вещества не существует, его используют лишь для удобства составления химических уравнений реакций.
Раствор SO2 в воде, имеет кислую среду. Такому раствору присущи все свойства кислот, в том числе реакция нейтрализации.
Сернистая кислота (или правильнее сказать - раствор сернистого газа в воде) образует два вида солей: сульфиты и гидросульфиты. Эти соли являются восстановителями.
Н2SO3 + NaOH → NaНSO3 + Н2O - такая реакция протекает при избытке сернистой кислоты
Н2SO3 + 2NaOH → Na2SO3 + 2Н2O - а эта реакция протекает при избытке едкого натра
Сернистая кислота обладает отбеливающим действием. Всем известно, что подобным действием обладает и хлорная вода. Но отличие заключается в том, что в отличии от хлора сернистый газ не разрушает красители, а образует с ними неокрашенные химические соединения!
Кроме основных свойств кислот сернистая кислота способна обесцвечивать раствор марганцовки по следующему уравнению:
5Н2SO3+2KMnO4 → 2 Н2SO4 +2MnSO4+K2SO4+Н2O
В этой реакции образуется бледно-розовый раствор, состоящий из сульфатов калия, марганца. Окраска обусловлена именно сульфатом марганца.
Сернистая кислота способна обесцветить бром
Н2SO3 + Br2 + Н2O → Н2SO4 + 2HBr
В этой реакции образуется раствор, состоящий сразу из 2-х сильных кислот: серной и бромной.
Если хранить сернистую кислоту при доступе воздуха, то этот раствор окисляется и превращается в серную кислоту
2Н2SO3 + O2 → 2Н2SO4
 Перейти на английский
Перейти на английский