Что такое и откуда берётся натуральный шёлк?!
Впервые о натуральном шёлке заговорили ещё в древнем Китае в 3-м тысячелетии до нашей эры. Существует легенда, что однажды, прогуливаясь в цветущем весеннем парке на дочь китайского императора с дерева упал маленький блестящий комочек. Девушка заинтересовалась им и отнесла его к отцу. С того самого момента, когда возник интерес к чудным коконам и начало развиваться шелкопрядство.


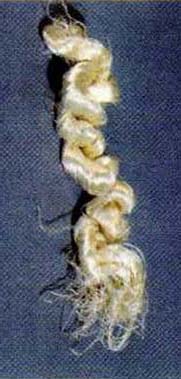
Белый блестящий комочек - это и есть тончайшие нити натурального шёлка. Его вьёт для себя гусеница тутового шелкопряда. Гусеница имеет два усика на голове, которые (как железы) вырабатывают выделения, которые застывают и превращаются в шёлковую нить.
Тутовый шелкопряд вьёт вокруг себя кокон диаметром около 2 см и длиной до 3,5 см. Толщина шёлковой нити составляет всего 0,02 мм, что в несколько раза тоньше волоса. Если размотать кокон тутового шелкопряда, то мы получим тончайшую нить около 3,5 км (3500 м). С такой толщиной нити, конечно же, работать не удобно, поэтому обычно перед работой завивают несколько нитей в одну.
Натуральный шёлк, как вы уже догадываетесь - это сложное органическое вещество белкового происхождения. Он состоит в основном из остатков молекул аминокислот, тирозина и анилина. Химическая формула натурального шёлка C15H23N5O6, что соответствует химическому веществе - фиброин (от латинского слова fibra - волокно).
В первоначальные этапы развития шелкопрядства использовали натуральное природное сырье - коконы шелкопрядов! И представьте, труд по размотки таких нитей не был механизирован. Но несмотря на то, что в середине уже 20-ого века были созданы механизмы по размотке коконов, цена шёлка всё равно снизилась незначительно! (для сравнения, за одну единицу шелкового изделия платили в 400 раз дороже, чем за пшеницу в таком же количестве по массе).
Предложение о получении искусственного шёлка впервые было изложено в научном труде одного из французских учёных (Рене Антуаном Реомюром) в середине 18 столетия. Изучая насекомых, он предложил, что можно химическим способом создать такой раствор, который бы позволил вытягивать из него тонкие нити, пригодные для станка. Но практически его идея была реализована только во второй половине 19 столетия французским химиком (Луи Шардонне)! Сырьём для изготовления искусственного шёлка служила целлюлоза и ещё одно сложное химическое вещество - полисахарид. Действуя азотной кислотой на эти материалы получали нитроцеллюлозу, химический состав которой (C6H7O2(OH)3_x(ONO2)x)n. Такое вещество можно растворить в смеси спирта и эфира и вытягивать из него тонкие волокна.
В начале 20 века его небольшая фабрика выпускала до 1000 тонн искусственного шёлка в год.
Луи Шардоне пропускал через очень тонкие трубки заранее подогретый раствор нитроцеллюлозы. Получавшиеся струйки попадали в холодную воду и там застывали в тонкие нити. Эти шёлковые нити автоматически наматывались на катушку. При добавлении в раствор нитроцеллюлозы какого-либо красителя можно получить искусственный шёлк различных цветов.
Позже технология была изменена: вместо воды использовался тёплый воздух, таким образом стало возможным экономить спирт и эфир. В последствии из нитроцеллюлозы стали получать пластмассу - целлулоид.
Нитроцеллюлоза - это вещество, которое прекрасно воспламеняется и горит, да и к тому же ещё обладает взрывоопасными свойствами. Это вещество может существовать в разных модификациях. В зависимости от числа нитрогрупп, входящих в нитроцеллюлозу, различают следующие вещества: коллоксилин ( с малым числом нитрогрупп), пироксилин (с увеличенным числом нитрогрупп). Полученные вещества широко применяют для изготовления динамита и бездымного пороха. Понятно, что одежда, изготовленная из нитроцеллюлозы мгновенно воспламенялась и сгорала!
В связи с горючими свойствами ткани был разработан метод перевода целлюлозы в раствор без применения азотной кислоты! Таким методом стало использование медно-аммиачного раствора (его называют прядильным раствором). Но что интересно, медно-аммиачный раствор не содержит ни одной молекулы аммиака и не содержит меди! Этот раствор был получен в середине 19 века Швейцарским учёным-химиком Маттиасом Эдвардом Швейцером. Он определил основы науки получения искусственного шёлка из медно-аммиачного раствора. Состав раствора - [Cu(NH3)4](OH)2 - гидроксид тетраамминмеди. Красивый тёмно-синий раствор обладает весьма необычными свойствами: при комнатной температуре он способен растворять хлопчатобумажную ткань и бумагу, шерсть, шёлк и, что особенно интересно, - растворяет даже волосы!
Но, как оказалось, несмотря на то, что крахмал и бумага - вещества близкие по химическому составу, но в отличие от бумаги, крахмал совсем не растворялся в полученной жидкости.

В середине 19 века был найден достаточно лёгкий способ химического получения гидроксид тетраамминмеда [Cu(NH3)4](OH)2. Если на мелкораздробленную медь действовать нашатырным спиртом (гидроксидом аммония NH4OH), то в результате химической реакции получалось то самое вещество синего цвета. При этом нужно было учитывать, чтобы реакция протекала при достаточном количестве кислорода (например, на открытом воздухе).
Химическая природа раствора гидроксид тетраамминмеда была изучена в середине 20 века. Медь, растворяясь в аммиаке, переходит в ионное состояние Cu2+, которое образует с аммиаком красивое комплексное химическое вещество аммиакат меди. В этом растворе также присутствует другой ион (анион) (С6Н8О5)2-n. Он находится только в растворе с выраженной сильнощелочной реакцией. Если на синий раствор подействовать какой-нибудь кислотой, то в результате химической реакции в осадок выпадает целлюлоза! Происходит следующая реакция:
nCu2++(С6Н10О5)n+2nОН- > [CuC6H8O5]n+2nH2O.
Получаемый красивый синий раствор гидроксид тетраамминмеди лёг в основу нового процесса по изготовлению искусственного волокна в промышленности. Первое получение в промышленных масштабах медно-аммиачного шёлка произошло к началу 20 века в Германии. Медно-аммиачный шёлк является искусственным волокном, но полученным из природного вещества - целлюлозы.

Как сделать шелковую нить в домашних условиях, используя при этом подручные средства?!
Поступим так. Приготовьте медный купорос CuSO4 и кальцинированную соду Na2CO3 (продаётся в хозяйственных магазинах, может также называться стиральной содой).
Готовим искусственный малахит! Конечно, не натуральный камень, хотя, с химической точки зрения – это тоже самое вещество). Готовим раствор медного купороса и раствор кальцинированной соды. Затем сливаем их и наблюдаем выпадение осадка, который и будет называться малахитом (с химической точки зрения).
Итак, когда осадок выпал, фильтруем его от жидкости. Затем осадок над растворить в концентрированном аммиаке (пропорция примерно так: 2 г осадка и 20 мл аммиака). Получаем темно-синий раствор гидроксид тетраамминмеди [Cu(NH3)4](OH)2, который был впервые получен в середине 19 столетия. Теперь готовим прядильный раствор. В полученный раствор вносим небольшие кусочки ваты. Вместо ваты можно использовать белую фильтровальную бумагу. Растворяем до тех пор, пока не получим достаточно вязкий раствор. А теперь самое интересное! Можно отлить немного этого прядильного раствора в пробирку, блюдце и добавить немного разбавленной соляной кислоты. Сразу можно увидеть выпадение осадка в виде белых хлопьев – это чистая целлюлоза!
Получим из раствора нить. В шприц набираем 10% процентный раствор серной кислоты H2SO4 и очень медленно выдавливаем его через иглу в прядильный раствор. Получаем настоящую нить. Её нужно подцепить пинцетом и поместить в воду. Для удобства такую работу лучше всего проводить в широких ёмкостях, имеющих низкие стенки. Теперь нить готова к использованию. Вот и всё! Аналогично готовят искусственный шёлк в промышленных масштабах. Отличием может быть то, что вместо темно-синего раствора используют другие прядильные растворы, при этом вместо целлюлозы используют её эфиры. В результате таких реакций образуются самые различные вискозные и ацетатные ткани.
 Перейти на английский
Перейти на английский