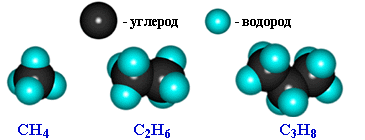
Предельные углеводороды - их название говорит за себя! Это сложные химические вещества, молекулы которых состоят из атомов водорода и атомов углерода.
Предельные углеводороды образуют гомологический ряд углеводородов, каждое химическое вещество в таком ряду отличается от предыдущего в химическом строении на одно и тоже количество атомов водорода и углерода.
Гомологический ряд углеводородов
- CH4 - метан
- C2H6 - этан
- C3H8 - пропан
- C4H10 - бутан
- C5H12 - пентан
- C6H14 - гексан
- C7H16 - гептан
- C8H18 - октан
- C9H20 - нонан
- C10H22 - декан ...
Гомологический ряд углеводородов характеризуется общей формулой, по которой можно определить формулу любого вещества данного ряда. Для предельных углеводородов - эта формула
CnH2n+2
C увеличением молекулярной массы вещества (увеличивается количество атомов углерода и водорода в молекуле) происходит увеличение температуры кипения этого вещества. Поэтому следует отметить, что вещества с CH4 по C4H10 - газы, с C5H12 по C15H32 - жидкости, далее - это твёрдые вещества!
Предельные углеводороды имеют ещё несколько названий - насыщенные углеводороды или парафины.
Предельные углеводороды образуют изомеры - вещества, которые имеют одинаковое число атомов одних и тех же элементов, но разное пространственное строение. Например, группа CH3 (или метил), может соединяться не с первым, а со вторым или третьим атомом водорода.
Изомеры характерны для предельных углеводородов, начиная с C4H10 - бутана.
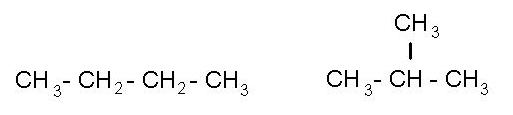
Слева - формула газа - бутан, справа - тот же бутан, только в форме изомера.
Если от предельного углеводорода отсоединить один атом водорода - то образуется очень активное химическое вещество, которое, практически, не существует в свободном состоянии, мгновенно вступает в реакцию.
В химическом отношении при комнатной температуре все алканы инертные (то есть не вступают в химические реакции). Но при повышении температур - проявляют достаточную химическую активность.
Свойства предельных углеводородов
- реакция замещения: (реакция галогенирования)
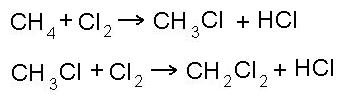
- реакция нитрования:
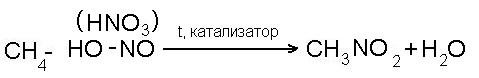
- реакция дегидрогенизации (отщепление водорода):
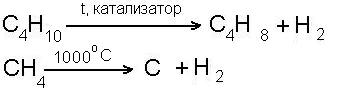
- реакция горения
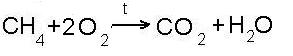
- реакция крекинга (расщепление большой молекулы на более мелкие молекулы)
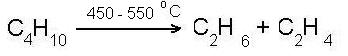
 Перейти на английский
Перейти на английский